В ПГУ смогут ускорить заживление ран
 В подведомственном Минобрнауки России Пензенском государственном университете медики запатентовали инновационный способ стимуляции заживления ран. Он подойдет для ран любых локализаций, форм и размеров. Для этого они используют современные скаффолд-технологии. Авторам удалось в 1,5 раза ускорить процесс репарации. В настоящее время технологию продолжают тестировать на лабораторных животных. В скором времени пройдут клинические исследования на базе Пензенской областной клинической больницы имени Н. Н. Бурденко. Об этом написало интернет-издание «Газета.ru».
В подведомственном Минобрнауки России Пензенском государственном университете медики запатентовали инновационный способ стимуляции заживления ран. Он подойдет для ран любых локализаций, форм и размеров. Для этого они используют современные скаффолд-технологии. Авторам удалось в 1,5 раза ускорить процесс репарации. В настоящее время технологию продолжают тестировать на лабораторных животных. В скором времени пройдут клинические исследования на базе Пензенской областной клинической больницы имени Н. Н. Бурденко. Об этом написало интернет-издание «Газета.ru».
Любые раны (операционные, случайные, умышленные, боевые) могут сопровождаться разнообразными осложнениями и после нанесения увечья, и в отдаленные сроки. Даже небольшой порез и царапина нуждаются в правильном уходе и лечении.
Рана — это нарушение целостности кожи и слизистых оболочек механическим воздействием. Как правило, оно сопровождается повреждением глубже лежащих тканей или органов. Человек испытывает болевые ощущения, а организм направляет все силы на восстановление и заживление места повреждения. Длительность восстановления нарушения зависит от характера и глубины повреждения, общего состояния организма.
Один из разработчиков способа, д-р мед. наук, профессор кафедры «Хирургия» Медицинского института ПГУ Константин Сергацкий рассказал, что длительный процесс заживления ран доставляет массу неудобств пациентам. Кроме того, любое повреждение, начиная от небольшой царапины и заканчивая обширными ранами, требует постоянных и своевременных перевязок. Это, в свою очередь, накладывает на медицинский персонал дополнительную нагрузку. По его словам, ускорение регенерации поврежденных тканей смогло бы упростить течение болезни у пациентов и избавить медицинских работников от лишней нагрузки.
В ПГУ предложили инновационный способ, ускоряющий заживление в 1,5 раза. Научный коллектив — д-р мед. наук, профессор кафедры «Хирургия» Медицинского института Константин Сергацкий, д-р мед. наук, профессор кафедры «Хирургия» Валерий Никольский, студентка Медицинского института Валерия Романова, канд. мед. наук, ассистент кафедры «Хирургия» Артем Захаров, канд. мед. наук, доцент кафедры «Хирургия» Александр Шабров, аспирант Медицинского института Михаил Миронов — предложил использовать для ускорения репарации внеклеточный коллагеновый матрикс в виде коллагенового геля и листовой формы. Исследователи совместили скаффолд-технологию и ранозаживляющее вещество. Предложив, по своей сути, новый способ введения лекарственного средства.
Внеклеточный матрикс находится в основе соединительной ткани в организме и выполняет функцию каркаса, а также коммуникации клеток между собой. Профессор Константин Сергацкий пояснил, при повреждении тканей собственный внеклеточный матрикс формируется в зоне раны, но, порой, усилий организма бывает недостаточно. Поэтому процесс заживления затягивается и возникают неблагоприятные последствия.
Для того чтобы помочь организму пензенские ученые предлагают использовать скаффолд-технологии. Поясним. Скаффолд-технология — это биоинженерная технология культивирования клеток на 3D-матрицах естественного или искусственного происхождения для пространственного ориентирования будущей ткани или органа с целью трансплантации.
«Ключевая роль скаффолд-технологий состоит в направлении роста клеток, что позволяет положительно влиять на течение раневого процесса», — поделился Константин Сергацкий.
Отметим, технология применения внеклеточного коллагенового матрикса известная. В ПГУ первыми предложили совместить использование природного внеклеточного коллагенового матрикса и ранозаживляющего вещества в одной технологии.
«Внеклеточный коллагеновый матрикс сам по себе оказывает положительное влияние на репаративные механизмы за счет стимуляции неоангиогенеза (процесса образования новых сосудов), а также роста соединительной и эпителиальной тканей. В дополнении к этому мы усилили его лекарственным препаратом на основе диоксометилтетрагидропиримидина (Метилурацилом®). Он способствует очищению раны, создает обезболивающее, противовоспалительное, антиоксидантное, иммуностимулирующее и мембраностабилизирующее воздействия. Поэтому формируется эффект, приводящий к ускорению заживления раны», — добавил ученый.
 Внеклеточный коллагеновый матрикс производится из подслизистой основы тонкой кишки свиньи и представляет собой природный бесклеточный ксеногенный биоматериал. Он содержит коллаген разных типов, глюкопротеины, гликозоаминогликаны и факторы роста клеток. При имплантации на рану со временем он «заселяется» собственными клетками реципиента. Таким образом, материал является своеобразной матрицей для формирования новых тканей, играющих немаловажную роль в процессе регенерации.
Внеклеточный коллагеновый матрикс производится из подслизистой основы тонкой кишки свиньи и представляет собой природный бесклеточный ксеногенный биоматериал. Он содержит коллаген разных типов, глюкопротеины, гликозоаминогликаны и факторы роста клеток. При имплантации на рану со временем он «заселяется» собственными клетками реципиента. Таким образом, материал является своеобразной матрицей для формирования новых тканей, играющих немаловажную роль в процессе регенерации.
Лечебная процедура проходит следующим образом. После очищения раны и появления на ней грануляционной ткани наносится гель из внеклеточного коллагенового матрикса, импрегнированного («насыщенного», «пропитанного») Метилурацилом®. Затем поверх укладывают листовую форму внеклеточного коллагенового матрикса, также импрегнированного упомянутым лекарственным препаратом.
Еще одна из особенностей разработки — технология применима к ранам любых размеров, так как листовая форма подбирается в соответствии с площадью раневой поверхности индивидуально.
Далее на рану накладывается асептическая повязка. Следующая перевязка проходит не ранее чем через три дня.
«Этого времени достаточно для того, чтобы внеклеточный коллагеновый матрикс, „насыщенный” Метилурацилом®, надежно зафиксировался на раневой поверхности. Это позволит снизить нагрузку и на медицинский персонал. В ежедневных перевязках не будет необходимости», — уверен Константин Сергацкий.
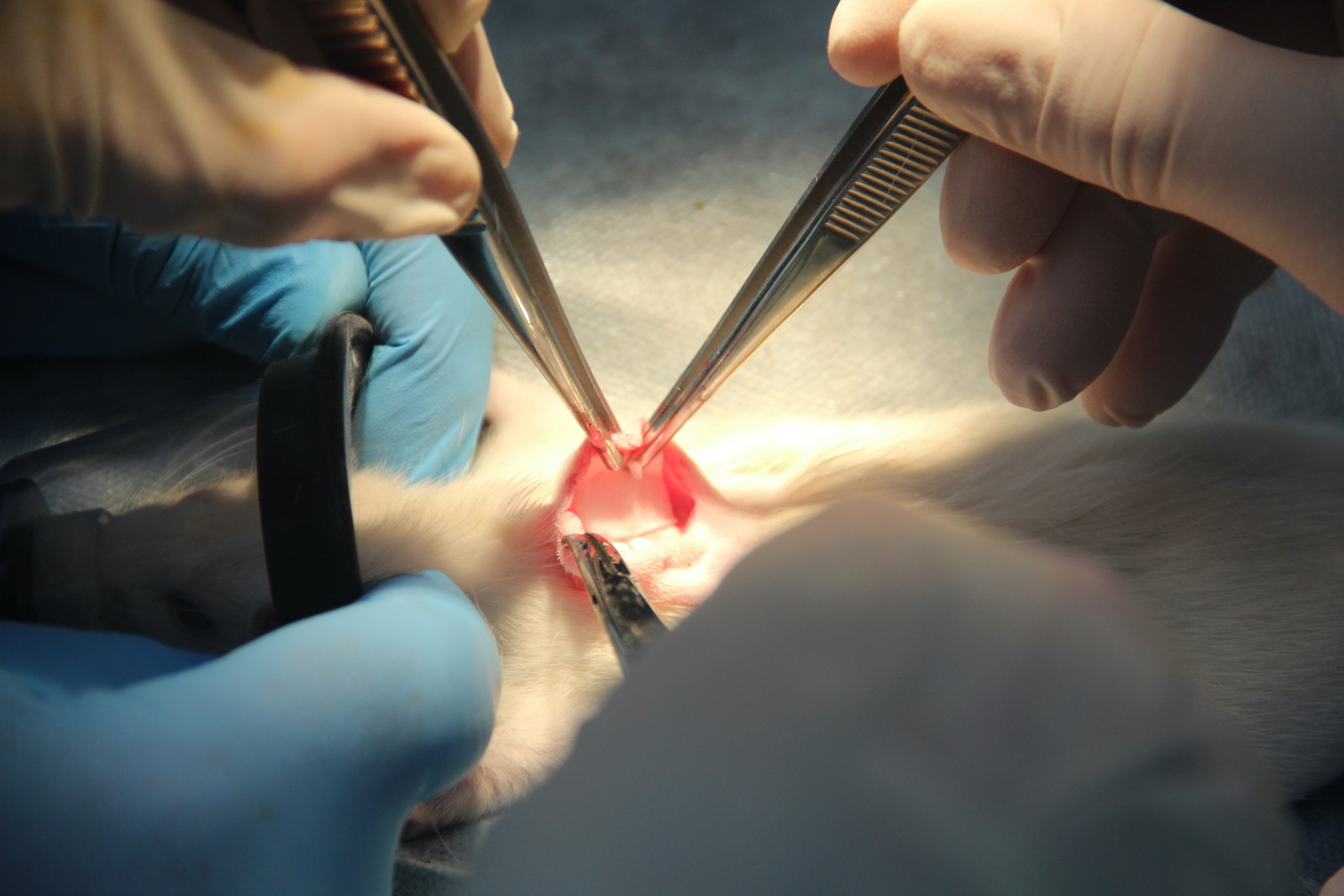
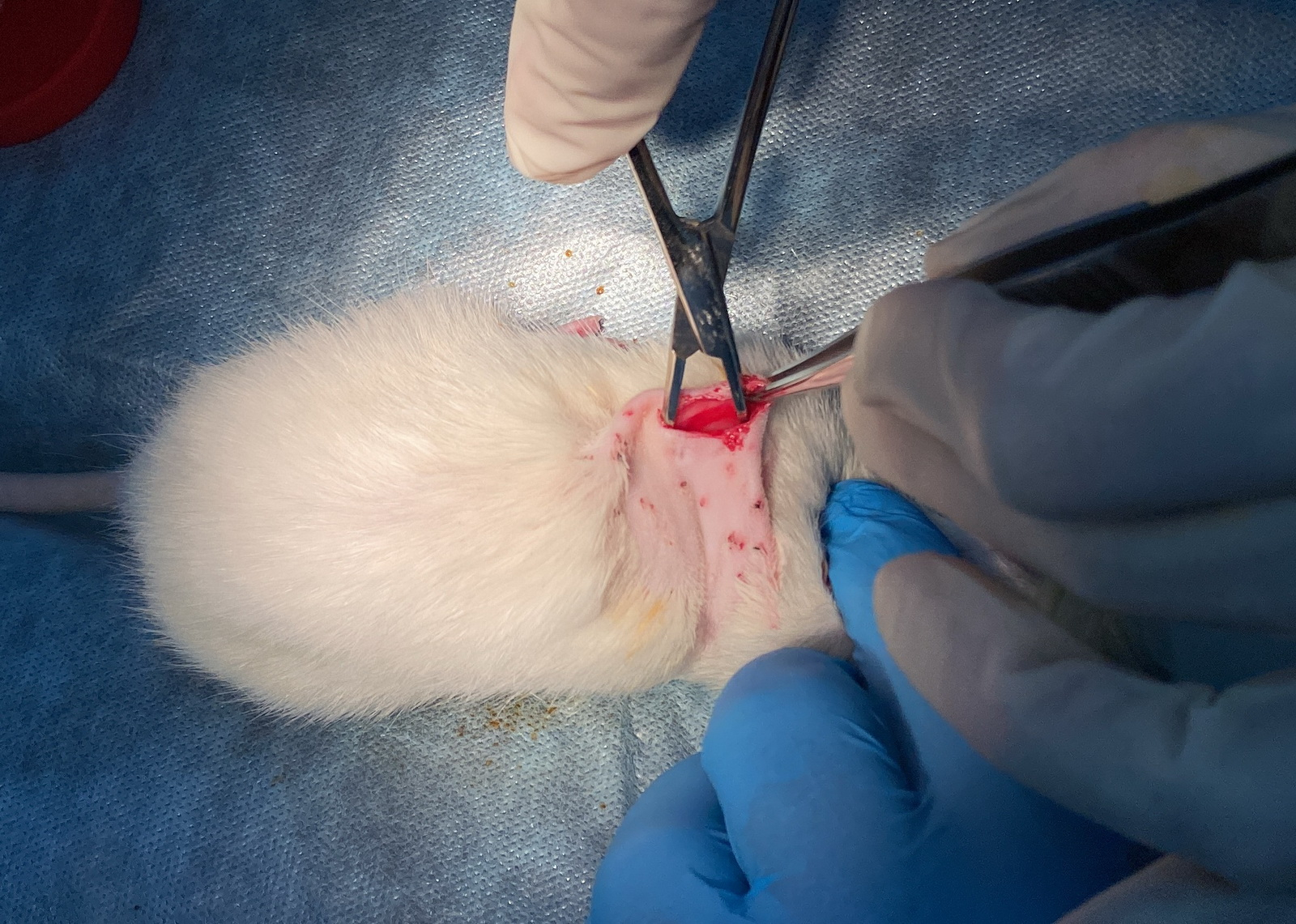 Способ был проверен на модели инцизионных (полученных путем иссечения тканей) ран на лабораторных животных — крысах — на базе Центра доклинических исследований Технопарка высоких технологий г. Пензы. Эксперимент показал, что через трое суток коллагеновый гель на основе внеклеточного матрикса, импрегнированного лекарственным препаратом, полностью впитался. А через шесть дней листовая форма надежно зафиксировалась. Меньше чем через две недели (12 суток) была достигнута полная эпителизация раневого дефекта. Противопоказаний способ не имеет.
Способ был проверен на модели инцизионных (полученных путем иссечения тканей) ран на лабораторных животных — крысах — на базе Центра доклинических исследований Технопарка высоких технологий г. Пензы. Эксперимент показал, что через трое суток коллагеновый гель на основе внеклеточного матрикса, импрегнированного лекарственным препаратом, полностью впитался. А через шесть дней листовая форма надежно зафиксировалась. Меньше чем через две недели (12 суток) была достигнута полная эпителизация раневого дефекта. Противопоказаний способ не имеет.
«Наше предложение значительно улучшит результаты лечения пациентов с ранами любого происхождения, то есть полученных от различных причин. А появиться они могут из-за механического воздействия, хирургического вмешательства, термического или химического ожога», — поделился Константин Сергацкий.
В планах ученых — продолжить исследование и сотрудничество с крупным производителем имплантируемых биоматериалов ООО «Кардиоплант». Отметим, комбинированные образцы предоставила эта компания.
На разработку получен патент Российской Федерации на изобретение, а проведение исследования одобрено Локальным комитетом по этике при ПГУ. В скором времени на базе Пензенской областной клинической больницы имени Н. Н. Бурденко способ пройдет свою клиническую апробацию.







 Версия для печати
Версия для печати